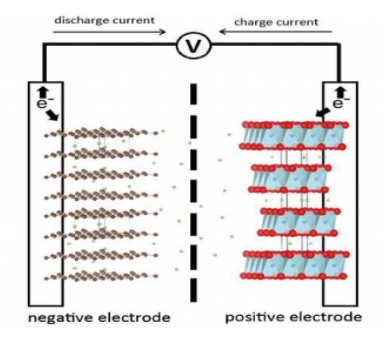
镍镉电池
当环境温度低时,使用密度为1.19至1.21(在15℃下)的氢氧化钾溶液。当温度低于-15℃时,使用密度为1.25至1.27(在15℃)的氢氧化钾溶液。
为了平衡低温性能和电荷保持能力,密封的镍镉蓄电池使用密度为1.40(在15℃下)的氢氧化钾溶液。为了增加电池的容量和循环寿命,通常将少量氢氧化锂(每升电解质约15至20g)加入电解质中。
在镍镉电池充电后,正极板上的活性材料变为氢氧化镍[NiOOH],负极板上的活性材料变为金属镉;在镍镉电池放电后,正极板上的活性材料变为羟基氧化镍。负极板上的活性材料变为氢氧化镉。
放电过程中的化学反应(1)负反应负极上的镉失去两个电子,成为二价镉离子Cd2 +,然后立即与溶液中的两个氢氧根离子OH-结合形成氢氧化镉。 Cd(OH)2沉积在负极板上。
(2)正极反应正极板上的活性材料是氢氧化镍(NiOOH)晶体。镍是正三价离子(Ni3 +),并且晶格中的每两个镍离子可以从外部电路获得从负电极转移的两个电子,以形成两个二价离子2Ni2 +。
同时,溶液中每两个水分子离子化的两个氢离子进入正极板并与晶格上的两个氧负离子结合形成两个氢氧根离子,然后与晶体上的两个氢离子结合。格子。
氢氧根离子与氢氧根离子一起形成两个氢氧化镍晶体。充电时的化学反应充电时,电池的正极和负极分别连接到充电器的正极和负极,电池的内部反应与放电时的内部反应完全相反,即发生负极的还原反应,发生正极的氧化反应。
(1)负极充电时负极板上的氢氧化镉首先被电离成镉离子和氢氧根离子,然后镉离子从外部电路获得电子,镉原子附着在板上,氢氧根离子进入。该溶液参与正极反应。
(2)正极反应在外部电源的作用下,在正极板上的氢氧化镍晶格中,两个二价镍离子各自失去一个电子,产生三价镍离子,同时,两个氢氧根离子在晶格中各自释放氢离子,在晶格上留下氧阴离子,释放的氢离子与溶液中的氢氧根离子结合形成水分子。然后,将两种三价镍离子与两种氧阴离子和剩余的两种氢氧根离子结合,形成两个氢氧化镍晶体。
当电池充电时,充电电流将导致电池中的水分解,并且在正极板和负极板上将分离大量的氧和氢。从上述电极反应可以看出,氢化氢或氢氧化钾不直接参与反应,而只是导电。
从电池反应的观点来看,在充电过程中产生水分子,并且在放电过程中水分子被消耗。因此,充电和放电期间的电解质浓度变化很小,并且密度计不能检测充电和放电的程度。